《临床医学研究与实践》作为现代医学领域的重要学术平台,承载着推动临床医学创新、转化医学发展和提升医疗服务质量的核心使命,其内容体系涵盖了从基础医学研究到临床应用的完整链条,强调以患者为中心,通过多学科协作解决临床实际问题,为医学进步提供理论与实践支撑。

临床医学研究的核心范畴与价值
临床医学研究是以疾病防治、健康促进为目标,通过科学方法探索人体生理病理规律、评估诊疗措施有效性与安全性的系统性工作,其核心范畴包括疾病机制研究、诊断技术优化、治疗方案创新、预后评估模型构建等,在肿瘤领域,从分子分型研究到靶向药物开发,再到免疫治疗方案的优化,每一步都依赖于严谨的临床研究,这类研究不仅为个体化医疗提供依据,还能通过循证医学证据推动诊疗指南的更新,最终改善患者预后,据世界卫生组织统计,高质量的临床研究可使重大疾病的死亡率降低15%-30%,凸显了其在医学进步中的关键作用。
研究方法与实践路径的规范化
临床医学研究的科学性依赖于规范的方法学设计,随机对照试验(RCT)是评价干预措施金标准的方案,通过随机分组、盲法评估和对照设置,减少选择偏倚和混杂因素影响,在评价某新型降压药的有效性时,研究者需将受试者随机分为试验组和对照组,分别给予新药和常规治疗,通过比较血压控制率、不良反应发生率等指标得出结论,观察性研究(如队列研究、病例对照研究)在罕见病研究或长期预后评估中具有不可替代的作用,真实世界研究(RWS)近年来兴起,通过收集真实医疗环境中的数据,弥补传统RCT在广泛人群适用性上的不足,研究过程中,需严格遵守《赫尔辛基宣言》伦理原则,通过伦理委员会审查,确保患者知情同意权与数据安全。
转化医学:从实验室到临床的桥梁
转化医学强调基础研究成果向临床应用的快速转化,实现“bench to bedside”的双向反馈,CRISPR-Cas9基因编辑技术在基础研究中取得突破后,迅速被应用于镰状细胞贫血的临床试验,通过纠正患者造血干细胞的基因缺陷达到治疗目的,转化医学的成功依赖于多学科团队协作,包括临床医生、基础研究员、生物统计学家、制药企业等,以糖尿病治疗为例,研究人员首先发现肠促胰素(如GLP-1)的降糖机制,随后开发出GLP-1受体激动剂类药物,最终成为临床一线治疗药物,这种“发现-开发-应用”的模式,极大缩短了理论到实践的距离。
数据科学与人工智能在临床研究中的应用
随着大数据技术的发展,临床医学研究进入精准化、智能化新阶段,电子健康记录(EHR)、基因组学数据和医学影像构成的多模态数据,为疾病预测模型提供了丰富素材,利用机器学习算法分析糖尿病患者视网膜图像,可实现糖尿病视网膜病变的早期筛查,准确率可达90%以上,人工智能在药物研发中的应用同样显著,通过深度学习分析化合物结构与活性关系,可将药物靶点发现时间从传统的5-6年缩短至1-2年,数据隐私保护、算法可解释性等问题仍是当前面临的挑战,需通过技术手段与法规规范共同解决。
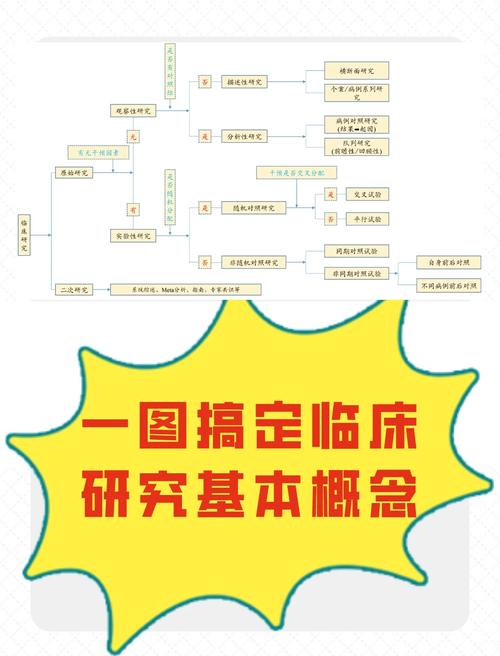
临床实践中的研究型思维培养
将研究型思维融入临床实践,是提升医疗服务质量的关键路径,临床医生可通过“发现问题-收集证据-实践验证-总结推广”的循环模式,推动诊疗方案的持续优化,某医院针对术后切口感染率较高的问题,通过回顾性研究发现血糖控制是独立危险因素,随后制定强化血糖管理方案,使感染率从8.3%降至3.1%,参与多中心临床研究、注册登记研究等,可帮助医生接触前沿进展,提升科研能力,我国《“健康中国2030”规划纲要》明确提出,要加强临床医学研究体系建设,培养一批兼具临床能力与科研素养的复合型人才。
挑战与未来发展方向
当前临床医学研究面临诸多挑战:研究资金投入不足、科研成果转化率低、临床医生科研能力参差不齐等,需从以下方向突破:一是加强基础研究与临床需求的对接,建立“临床问题导向”的立项机制;二是推动医企协同创新,通过产学研合作加速成果转化;三是完善科研评价体系,破除“唯论文”倾向,注重研究成果的临床价值与社会效益;四是加强国际合作,参与全球多中心临床试验,提升我国医学研究的国际影响力。
相关问答FAQs
Q1:临床医学研究与基础医学研究的区别是什么?
A:临床医学研究聚焦于疾病在人体中的发生发展规律、诊疗方法的优化及效果评估,直接服务于患者治疗与健康改善,以人为研究对象(或基于人体样本),强调实践应用;基础医学研究则以实验动物、细胞、分子等为对象,探索生命现象的本质与机制,为临床研究提供理论支撑,两者相辅相成,基础研究的突破往往推动临床诊疗的革新,而临床问题又为基础研究指明方向。
Q2:如何确保临床医学研究的伦理合规性?
A:确保临床研究伦理合规需从多层面入手:①研究设计需通过机构伦理委员会(IRB)或伦理审查委员会(ERC)的审查,评估风险-受益比;②严格遵守知情同意原则,确保受试者充分了解研究目的、流程及潜在风险后自愿参与;③涉及弱势群体(如儿童、精神疾病患者)的研究需额外保护措施;④研究过程中需设立数据安全监察委员会(DSMB),及时监测不良事件;⑤研究结束后需向伦理委员会提交总结报告,确保受试者权益持续得到保护,需遵循国际伦理准则(如《贝尔蒙报告》)及国家相关法律法规(如《涉及人的生物医学研究伦理审查办法》)。